看到了Wang et al. Cell Discovery (2022)的文章:《Single-cell dissection of remodeled inflammatory ecosystem in primary and metastatic gallbladder carcinoma》里面提到了: A small amount of PLA2G2A epithelial cells with copy number variation were identified from a histologically benign sample.
蛮有意思的,这个上皮细胞的特性是高表达PLA2G2A基因,但是它来源于非肿瘤组织,而且它居然是有拷贝数变异的!如下所示:
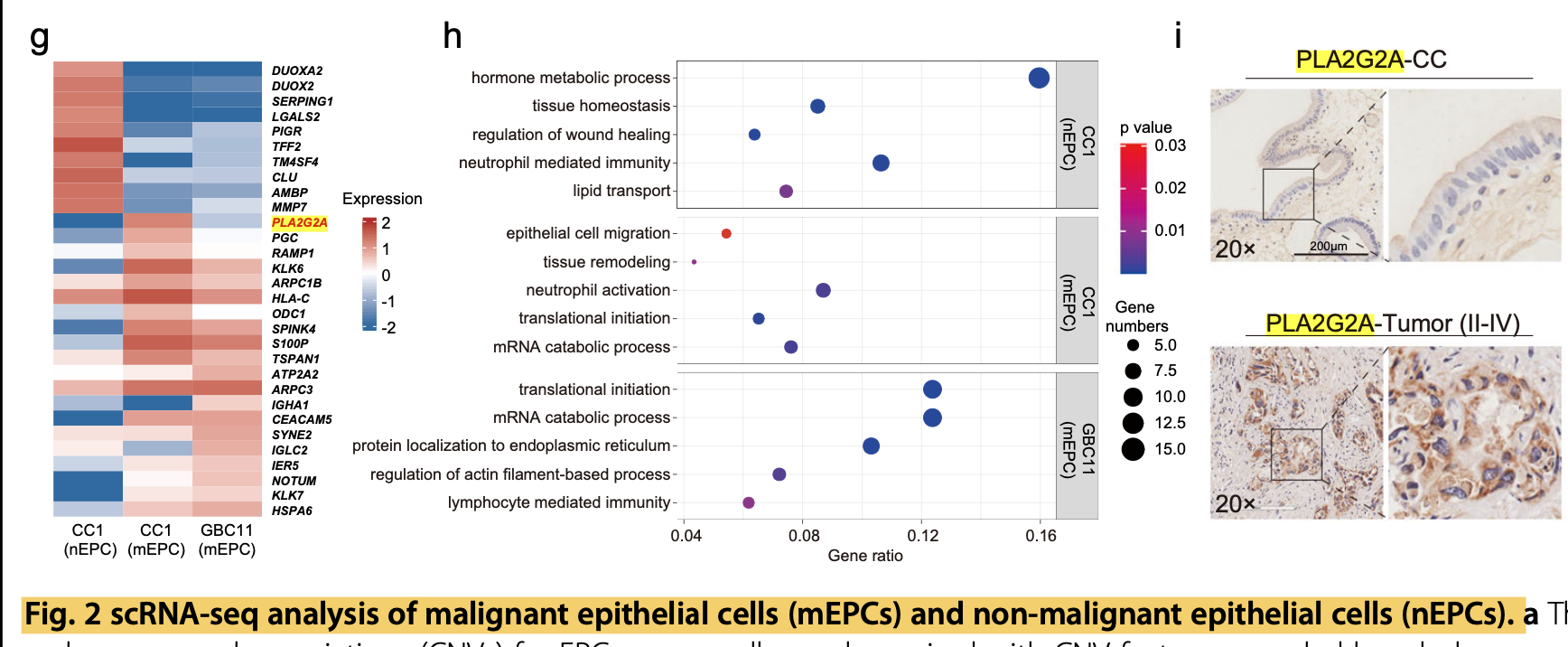
图例分别是:
- g Heatmap showing top-ranking DEGs for CC1-originated nEPCs, CC1-originated mEPCs, and GBC11-originated mEPCs.
- h Dot plots showing significantly enriched GO terms across CC1- originated nEPCs, CC1-originated mEPCs, and GBC11-originated mEPCs.
- i PLA2G2A expression across inflamed gallbladders (n = 17), GBCs in situ (Tis; n = 59), and GBCs (TNM II-IV; n = 48),
其中 CC是 chronic cholecystitis;
但是另外一个2022的NC文章:《Single cell profiling of primary and paired metastatic lymph node tumors in breast cancer patients》提到了:we identify a subtype of PLA2G2A+ cancer-associated fibroblasts enriched in HER2+ breast cancer patients that promotes immune infiltration. 如下所示:
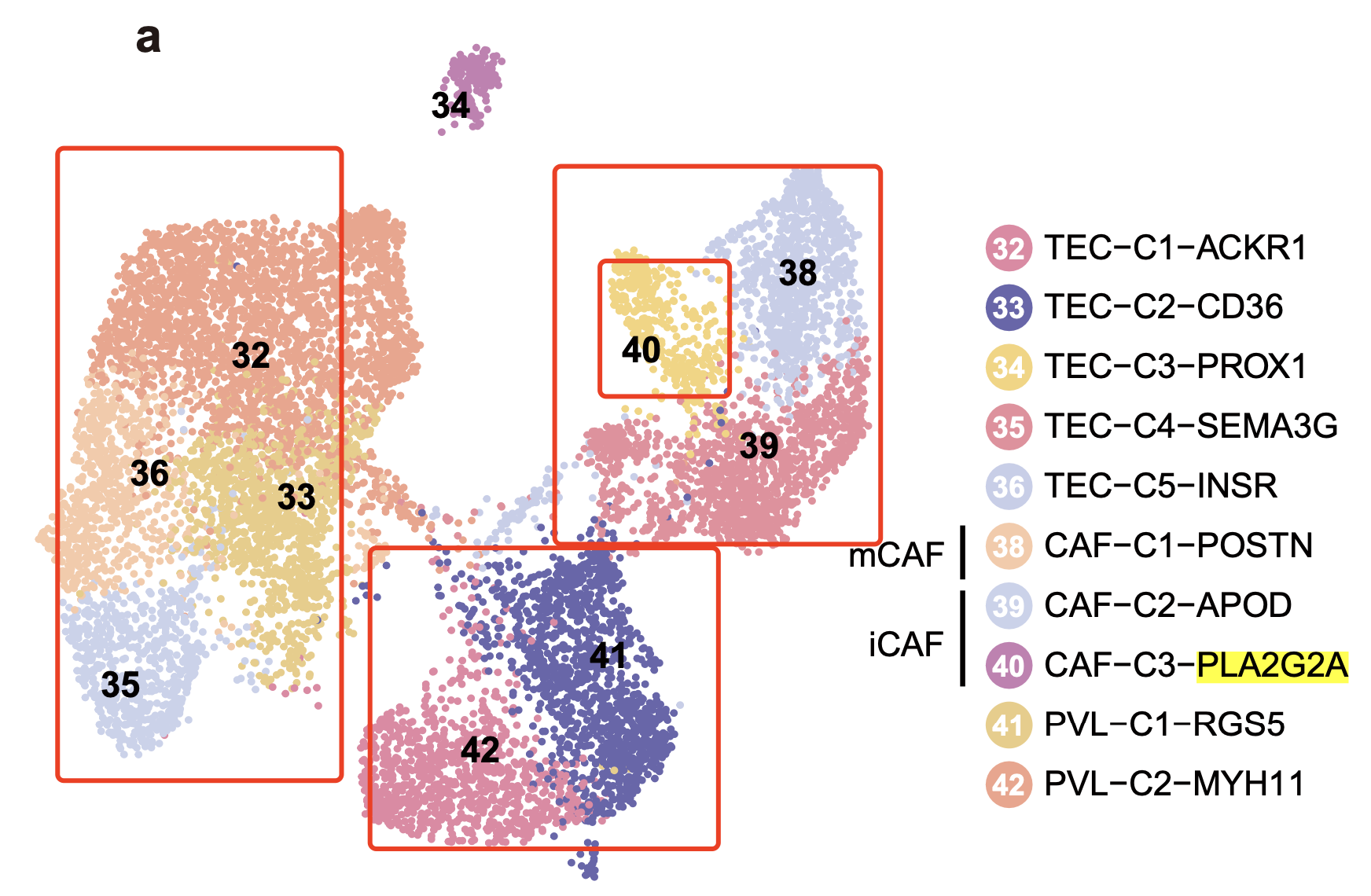
再比如2016的文章:《Secreted Phospholipases A2 Are Intestinal Stem Cell Niche Factors with Distinct Roles in Homeostasis, Inflammation, and Cancer》,提到了 The Pla2g2a gene is mainly, yet not exclusively, expressed in the small intestine and in particular by Paneth cells
在bulk水平也有很多研究,比如2023的一个上海交通大学学报(医学版)数据挖掘文章:《PLA2G2A在肾乳头状细胞癌中的表达及临床意义》,doi: 10.3969/j.issn.1674-8115.2023.02.003,提到了PLA2G2A在tcga和gtex数据库的表达量情况:
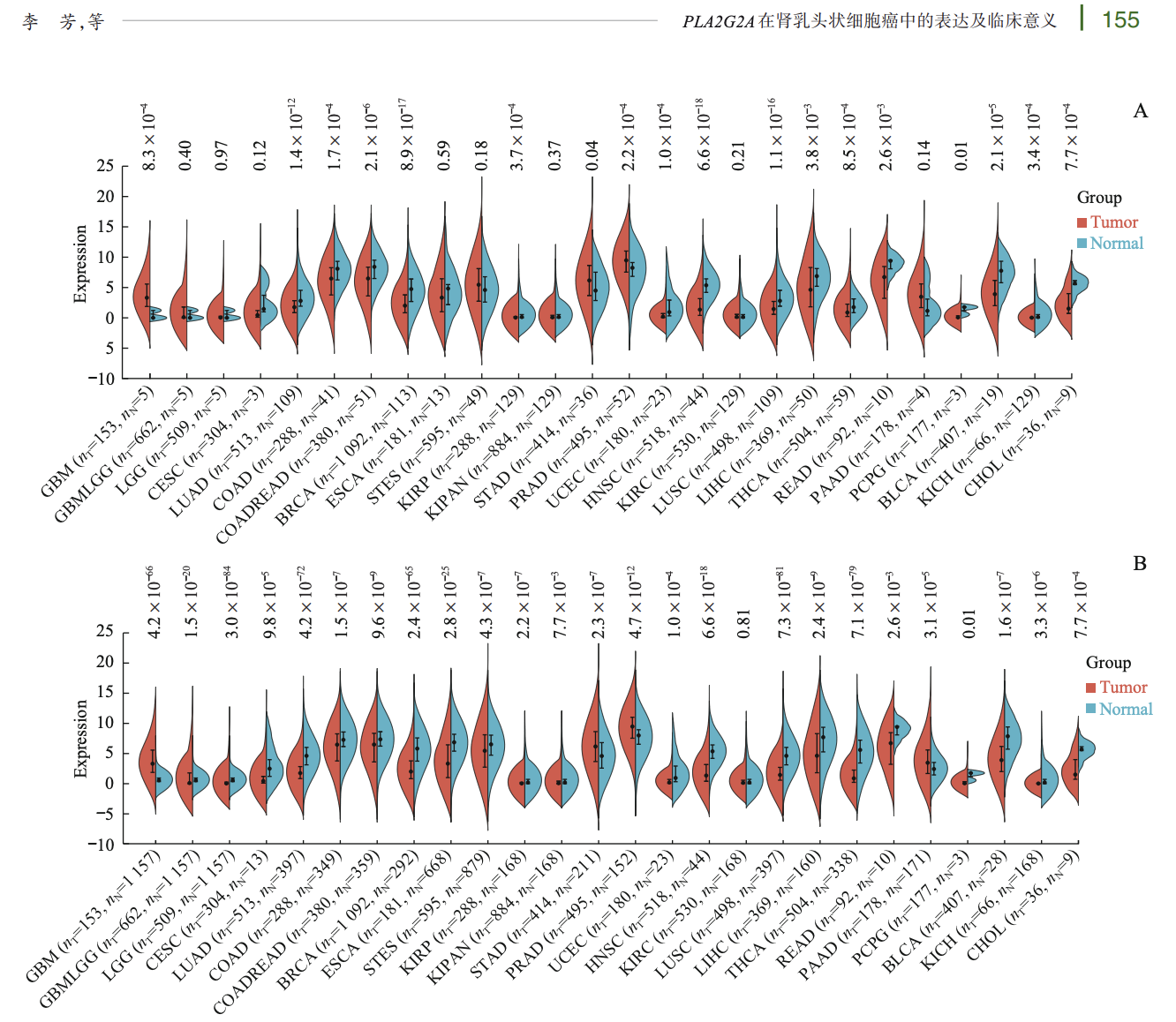
有一些基因会在一些单细胞亚群特异性的高表达
通常我们拿到了肿瘤相关的单细胞转录组的表达量矩阵后的第一层次降维聚类分群通常是:
- immune (CD45+,PTPRC),
- epithelial/cancer (EpCAM+,EPCAM),
- stromal (CD10+,MME,fibro or CD31+,PECAM1,endo)
参考我前面介绍过 CNS图表复现08—肿瘤单细胞数据第一次分群通用规则,这3大单细胞亚群构成了肿瘤免疫微环境的复杂。绝大部分文章都是抓住免疫细胞亚群进行细分,包括淋巴系(T,B,NK细胞)和髓系(单核,树突,巨噬,粒细胞)的两大类作为第二次细分亚群。但是也有不少文章是抓住stromal 里面的 fibro 和endo进行细分,并且编造生物学故事的。
这种基因在特定类型的细胞或细胞亚群中高表达的现象通常是由于这些基因的功能与该细胞类型或亚群的特定生理功能密切相关。这种特异性表达可以通过几种方式实现:
- 细胞分化和特异性转录因子调控: 在细胞分化过程中,特定类型的细胞会表达特定的转录因子,这些转录因子会调控特定基因的表达。例如,EPCAM基因在上皮细胞中高表达,可能是因为上皮细胞特异性的转录因子调控了EPCAM的表达。
- 细胞信号通路调控: 不同类型的细胞会参与不同的信号通路,这些信号通路可能会直接或间接地调控特定基因的表达。例如,PECAM在内皮细胞中高表达可能与内皮细胞的特定信号通路有关。
- 组蛋白修饰和染色质结构: 染色质的结构和组蛋白的修饰状态对基因的表达也有重要影响。特定类型的细胞可能具有特定的染色质状态,这可能导致某些基因在该类型的细胞中高表达。
- 表观遗传学调控: 表观遗传学调控包括DNA甲基化、组蛋白修饰和非编码RNA等调控机制,它们可以在细胞特异性基因表达中发挥关键作用。
因此,这些基因的特异性高表达往往是细胞类型和功能的直接反映,反映了细胞内复杂的调控网络和表观遗传学机制。
如果多个单细胞亚群都高表达同一个基因,那样特异性就大打折扣了。这种情况通常反映了该基因在多个细胞类型或亚群中都具有重要的功能或参与了多个细胞功能过程。这种现象可能是由于以下原因: - 基因多功能性: 有些基因可能在多个细胞类型或功能过程中发挥作用,因此它们可能会在多个单细胞亚群中高表达。
- 细胞类型相似性: 如果多个细胞亚群在基因表达模式上相似,或者它们共享相似的细胞功能,那么它们可能会共同高表达某些基因。
- 调控网络的复杂性: 调控网络可能会跨越不同的细胞类型或亚群,并影响相同的基因表达。这种情况下,即使细胞类型不同,也可能会观察到相同基因的高表达。
- 局部环境因素: 某些基因的表达可能受到细胞周围环境因素的影响,这些因素可能在不同细胞亚群中存在相似性,导致相同基因在多个细胞亚群中高表达。
比如你在很多单细胞亚群都可以看到,干扰素基因高表达,增值相关基因高表达,细胞应激相关基因高表达,金属离子酶基因高表达。但是PLA2G2A基因似乎并不是这些。
那么,问题来了,这个事情如何解释呢?是2022的两个文章的单细胞数据分析有误吗,还是背后有合理的生物学机制呢?