文章发表于2018年的《Nature Communications》 , 题目为“Profiling human breast epithelial cells using single cell RNA sequencing identifies cell diversity”。 作者从7个个体的乳腺上皮细胞提取25,790 个单细胞进行转录组测序。测序的原始数据都上传到了NCBI的GEO数据库: GSE113197.如下;

单细胞测序技术细节
作者采取了两种完全不同的测序建库技术
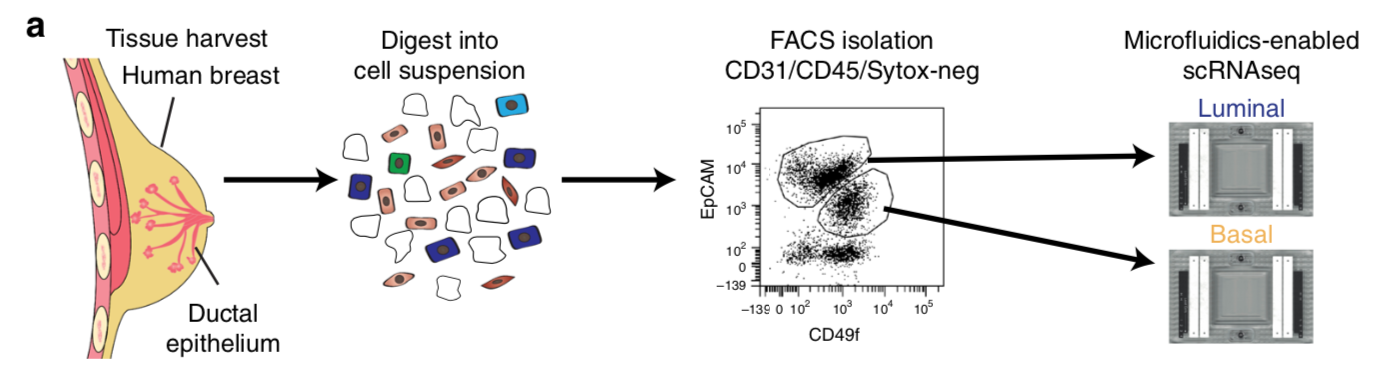
首先是 Fluidigm C1 microfluidics-enabled scRNAseq platform, 对3个人,消耗了13块芯片,测量了868 个细胞,平均1.6M的测序量,质控过滤后剩下703个单细胞,平均检测表达基因为4500个。
其中流式筛选细胞:
- basal (CD49f-hi, EPCAM+)
- luminal (CD49f+, EPCAM-hi)
然后是基于的droplet的高通量单细胞技术,对4个人,平均每个人测量5000个细胞,平均每个细胞的测序量是0.06M,虽然跟前面的Fluidigm C1 技术比起来微不足道,但是足够进行细胞分群了。 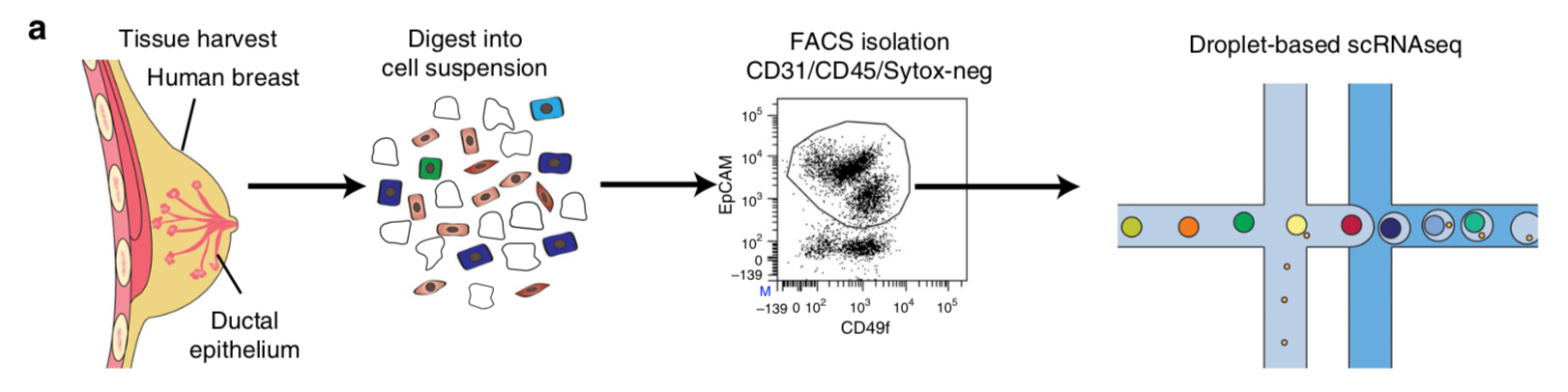
对C1数据集就自己使用RSEM处理流程得到RPKM表达矩阵,对10X数据就走 10× Genomics Cell Ranger套餐得到表达矩阵。
表达矩阵后续分析走的是Seurat流程,聚类可视化选tSNE,作者数据分析代码在https://github.com/kessenbrocklab/Nguyen_Pervolarakis_Nat_Comm_2018低通量单细胞转录组
对1,2,3这3个病人使用的是 Fluidigm C1 技术,低通量单细胞转录组,表达矩阵分析如下;
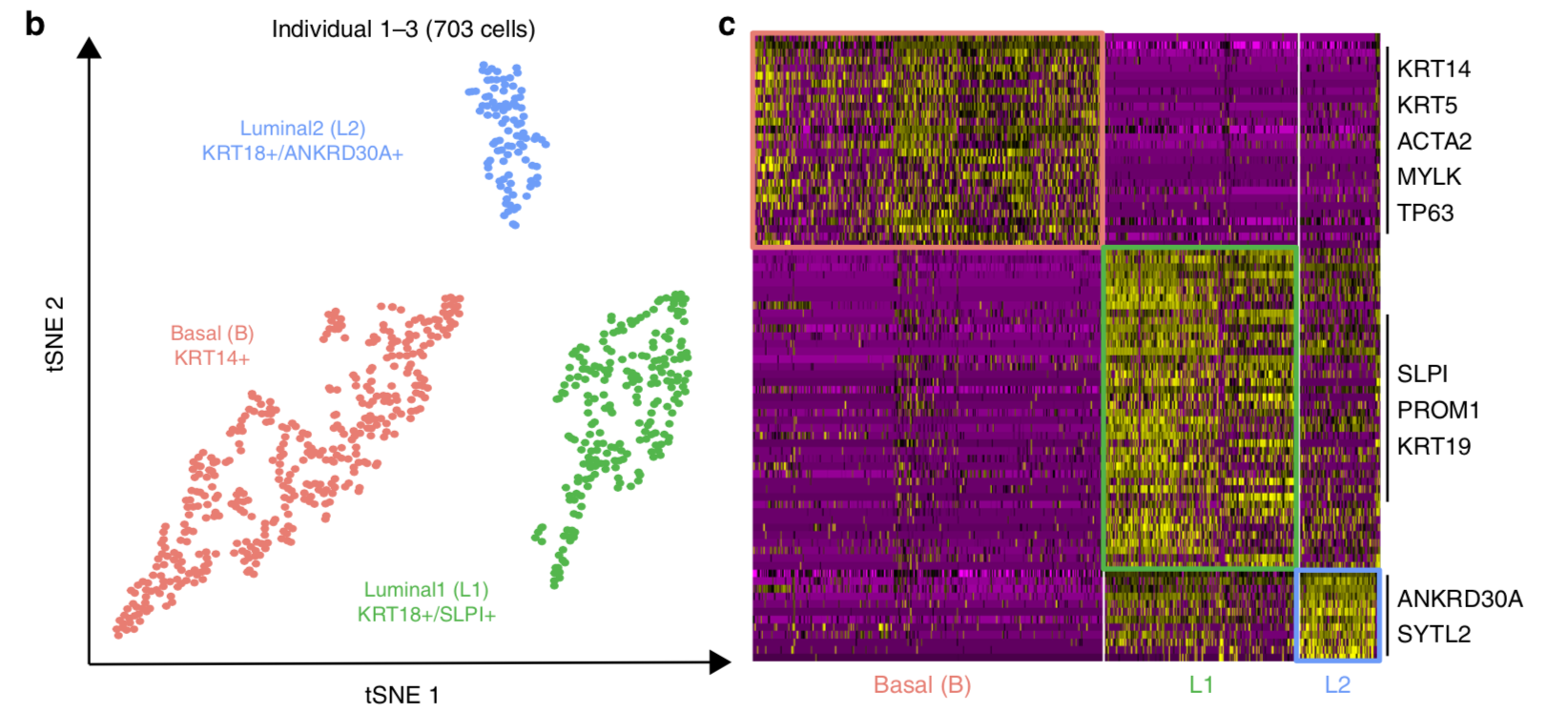
根据附件Supplementary Figure 1. d可以看到不同人的同一种细胞是聚在一起的,而且可以可视化相应的marker基因。
符合认知,鉴定出了三种不同的上皮细胞群:- 1种基底细胞
- 2种管腔细胞,即L1型和L2型
- L1型是分泌细胞
- L2型在乳腺组织内扮演激素敏感元件功能。
以前通常认为乳腺上皮包括两大类细胞:位于内层的分泌性管腔细胞(secretory luminal cells)和位于外层的基底/肌上皮细胞(basal/myoepithelial cells)。 单细胞转录组之前的技术还不足以在单细胞水平全局检测基因表达。高通量单细胞表达矩阵聚类
作者这里主要描述第4个人的细胞分群情况
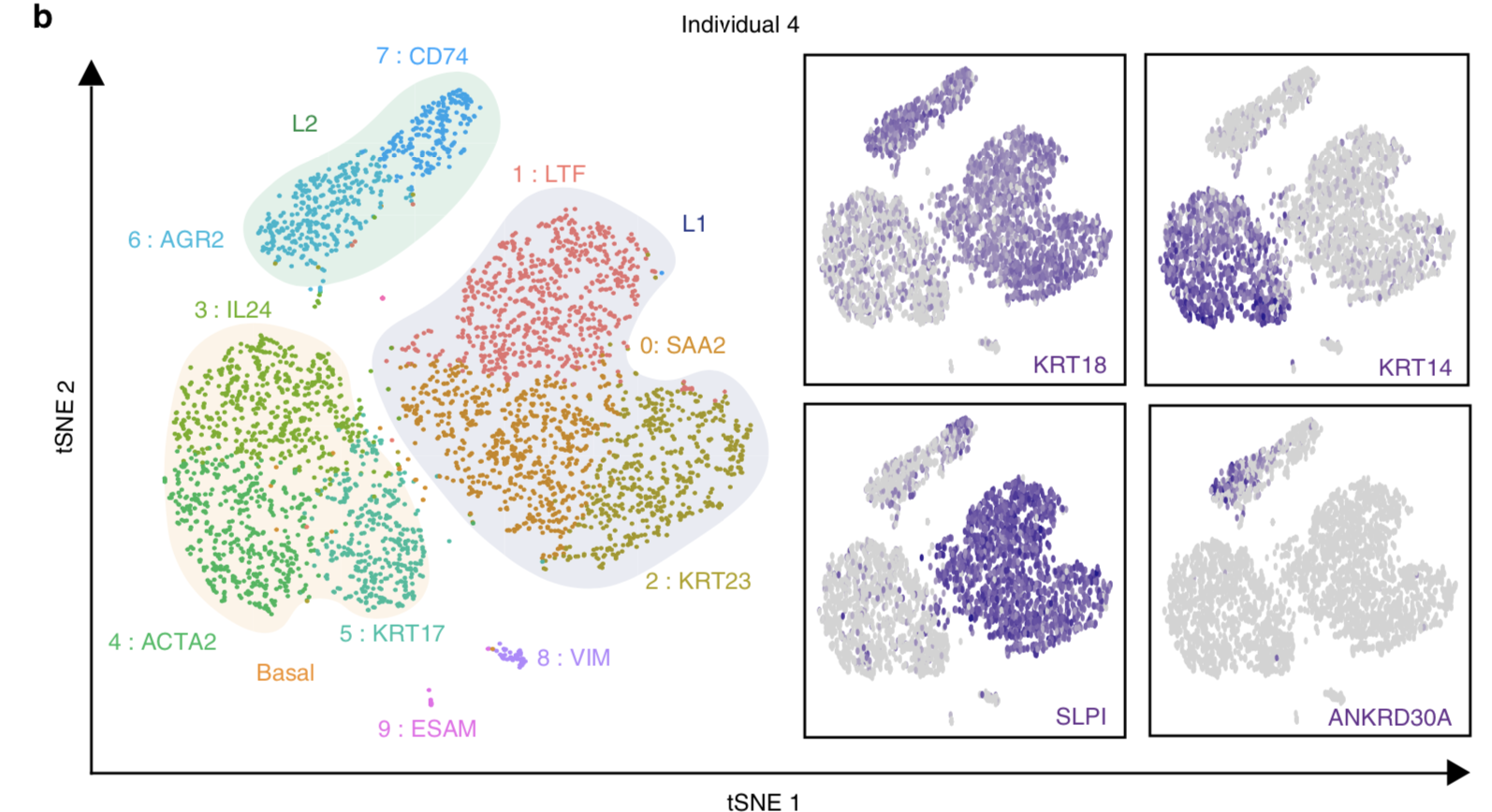
首先确定结论是10X的表达矩阵也可以得到在C1数据集相同的3个分类,如下:
- Basal (KRT14+)
- Luminal1 (L1; KRT18+/SLPI+)
- Luminal2 (L2; KRT18+/ANKRD30A+)
这3类主要的细胞类型,根据细胞状态的不同占据了 0~7这8个clusters。
也发现了一些非上皮细胞: - cluster 8 was defined by stromal marker VIM
- cluster 9 showed specific expression of endothelial marker gene ESAM
- cluster 10 included a small number of dispersed cells most likely representing outliers
细看3类亚群的深入分群
先看看基底细胞 Basal (KRT14+) 的细分情况:
- specific expression of inflammatory mediators (IL24;Cluster 3)
- markers for myoepithelial cell function (ACTA2; Cluster 4)
- specific epithelial keratin expression (KRT17; Cluster 5), respectively.
- ZEB1 and TCF4 代表着的基底细胞亚群能被C1去却不能被10X检测到,是单细胞建库技术的差异,可能是基因覆盖度区别。
再看看 luminal cell type L1 的细分情况: - milk production (LTF;Cluster 1)
- high expression of secretory molecules (SAA2;Cluster 0)
- distinct epithelial keratin expression (KRT23;Cluster 2).
最后看看 luminal cell type L2 的细分情况: - hormone responsive genes (AGR2; Cluster 6)
- specific cell surface markers (CD74; Cluster 7)
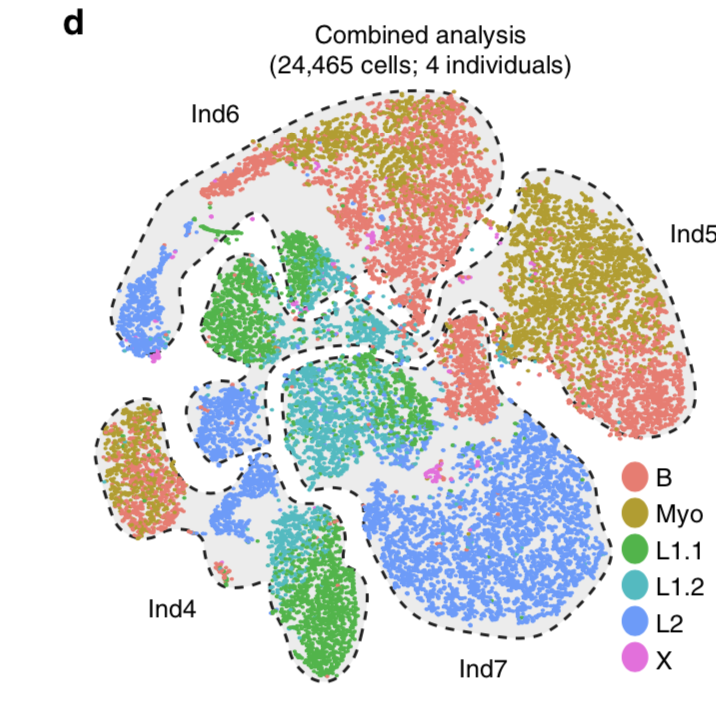
细胞分群,加上对应亚群的marker基因,是目前单细胞转录组数据分析的主要结果。不同人的细胞亚群比例
不同的个体的这些细胞状态比例差异很大,就是个体差异性,或者手术取样部位差异。
最后分群如下: - namely Basal (B),
- Myoepithelial (Myo),
- Luminal1.1 (L1.1),
- Luminal1.2 (L1.2),
- Luminal2 (L2),
- the small Unclassified (X)
这4个人的11群群细胞比例如下;
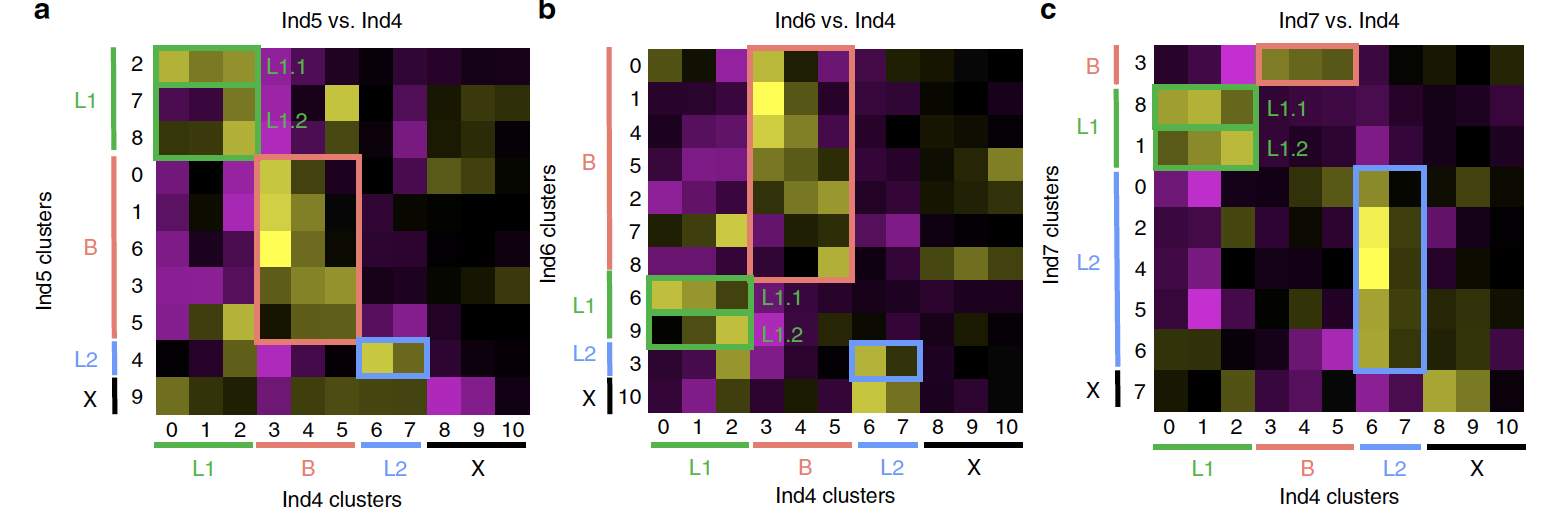
可以看到,不同人的11类细胞是可以互相印证的, 但是也有差异。
合并起来发现,这些细胞的个体差异居然是大于细胞分群差异的,很有可能是批次效应没有被去除掉。
重建乳腺发育过程
为了理解细胞类型及其状态之间的相互关系,通过拟时间排序重构了分化轨迹,这里使用Monocle对4个人的共4000个细胞进行分析。
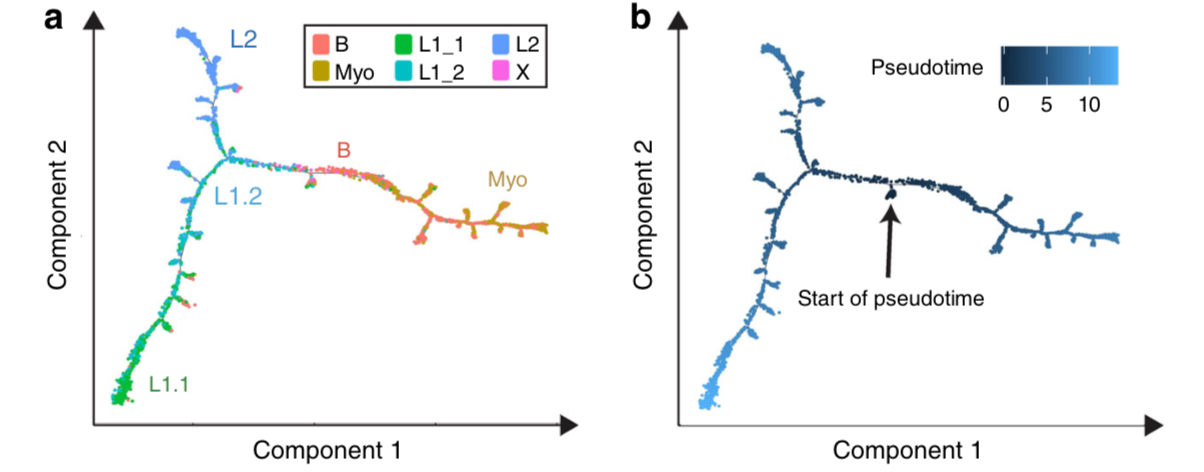
4个个体的样本群体产生了一个紧密相连的分化轨迹,分成三个主要分支,分别对应主要细胞类型Basal、L1和L2。这表明该系统是通过一个连续的谱系、而不是几个间断的谱系来维持的。文章意义
乳腺癌由乳腺上皮细胞遗传变异导致,遗传变化令乳腺组织细胞癌变,了解乳腺癌的早期起源,有潜力转化为癌症早期诊断方法,在疾病威胁生命之前构筑预防癌症第一道防线。
“我们对人体细胞多样性全谱还处于一知半解,特别是认识不同人类乳腺上皮细胞类型的知识盲点阻碍了我们研究不同细胞对癌症发生和发展的作用。新发现的三种上皮细胞类群填补了一部分知识漏洞,它将帮助我们了解乳腺癌系统的发展
这些不同的乳腺上皮细胞亚群可作为重建不同亚型乳腺癌起源的起点。
该研究由加州大学欧文分校(UCI)生物化学助理教授、生物医学研究员Kai Kessenbrock博士领导, Kessenbrock实验室与UCI研究员Devon Lawson博士和MD安德森的Nicholas Navin博士正在用类似方法全面地绘图人体组织所有细胞类型,他们的研究隶属于国际性的由Chan/Zuckerberg倡议资助的人类细胞地图(Human Cell Atlas)项目的一部分。一些疑问
其实之前也有大批量的单细胞数据,比如浙大的 40万单细胞小鼠图谱,也应该是有 好几万的乳腺上皮细胞,难道没有分类够细致吗?
后来看到的发育分享单细胞转录组文章多了,发现大家都会提到浙大的 40万单细胞小鼠图谱,但是因为他们做了太多器官,所以其实平摊到某个单独研究点来说,细胞数量并不大。