一.下载并安装这个软件
下载地址进下面,但是下载源码安装总是很困难,我直接下载bin文件可执行程序。
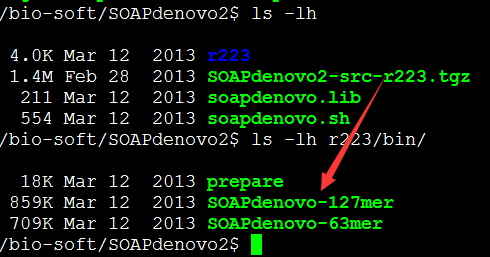
解压进入目录
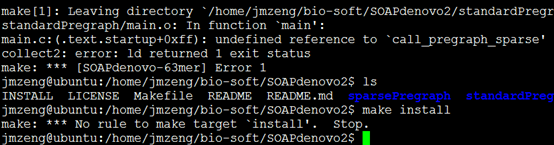
首先make
然后make install即可
安装总是失败,我也不知道怎么回事,懒得解决了。
直接去我老师那里把这个程序拷贝进来了。
https://github.com/aquaskyline/SOAPdenovo2/archive/master.zip
http://sourceforge.net/projects/soapdenovo2/files/SOAPdenovo2/bin/r240/SOAPdenovo2-bin-LINUX-generic-r240.tgz/download
http://sourceforge.net/projects/soapdenovo2/files/latest/download?source=files
也可以直接下载bin程序
二.准备测试数据
类似于这样的几个文库的左右两端测序数据。
我这里用一个小样本的单端数据做测试
三,参考命令
You may run it like this:
参考:http://www.plob.org/2012/07/06/2537.html
https://github.com/aquaskyline/SOAPdenovo2
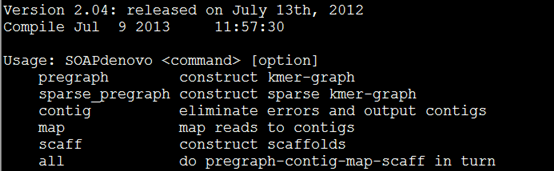
总共就四个步骤,介绍如下。
| ./pregraph_sparse [parameters] |
| ./SOAPdenovo-63mer contig [parameters] |
| ./SOAPdenovo-63mer map [parameters] |
| ./SOAPdenovo-63mer scaff [parameters] |
| i) preparing the pregraph. This step is similar to velveth for velvet. |
| ii) Determining contigs. This step is similar to velvetg for velvet. |
| iii) Mapping back reads on to contigs. |
| iv) Assembling contigs into scaffolds. |
| SOAPdenovo-63mer sparse_pregraph -s config_file -K 45 -p 28 -z 1100000000 -o outPG |
| SOAPdenovo-63mer contig -g outPG |
| SOAPdenovo-63mer map -s config_file -g outPG -p 28 |
| SOAPdenovo-63mer scaff -g outPG -p 28 |
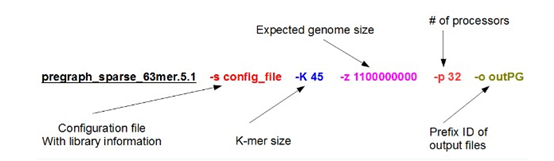
官网给出的步骤如下
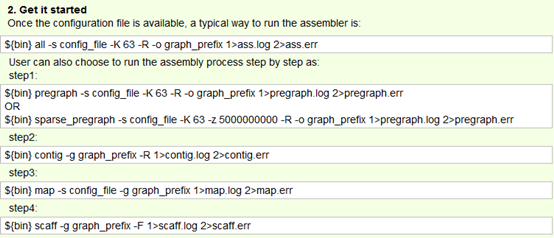
这个命令还需要一个配置文件
max_rd_len=99 设置最大reads长度,具体情况具体定义
[LIB] 第一个文库数据
avg_ins=225
reverse_seq=0
asm_flags=3
rank=1
q1=runPE_1.fq
q2=runPE_2.fq
[LIB] 第二个文库数据
avg_ins=2000
reverse_seq=1
asm_flags=2
rank=2
q1=runMP_1.fq
q2=runMP_2.fq
也可以全部一次性的搞一个命令
all -s config_file -K 63 -R -o graph_prefix 1>ass.log 2>ass.err
我简单修改了一下参考博客的代码跟官网的代码,然后运行了我自己的代码
/home/jmzeng/bio-soft/SOAPdenovo2-bin-LINUX-generic-r240/SOAPdenovo-127mer
all -s config_file -K 63 -R -o graph_prefix 1>ass.log 2>ass.err
反正我也不懂,就先跑跑看咯
我选取的是7个单端数据,所以我的配置文件是
max_rd_len=500
[LIB]
avg_ins=225
reverse_seq=0
asm_flags=3
rank=1
p=SRR072005.fa
p=SRR072010.fa
p=SRR072011.fa
p=SRR072012.fa
p=SRR072013.fa
p=SRR072014.fa
p=SRR072029.fa
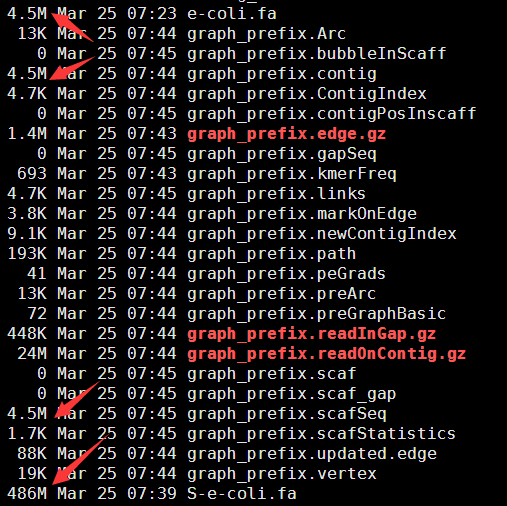
四.输出数据解读
好像我的数据都比较小,就7个三百多兆的fasta序列,几个小时就跑完啦
四个步骤都有输出数据
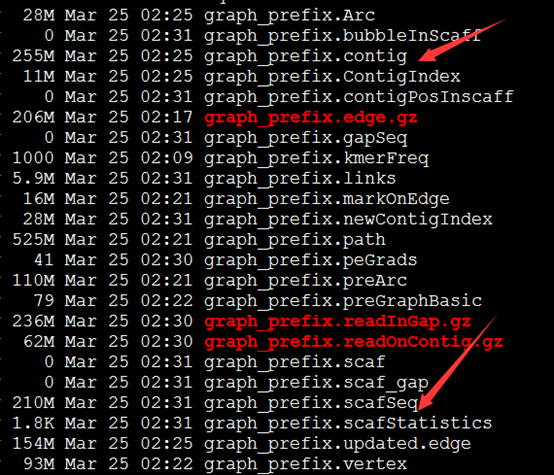
好像组装效果惨不忍睹呀!共86万的contig,50多万的scaffold
scaffolds>100 505473 99.60%
scaffolds>500 113523 22.37%
scaffolds>1K 48283 9.51%
scaffolds>10K 0 0.00%
scaffolds>100K 0 0.00%
scaffolds>1M 0 0.00%
这其实都相当于没有组装了,因为我的测序判断本来就很多是大于500的!
可能是我的kmer值选取的不对
Kmer为63跑出来的效果不怎么好,86万的contig,50万的scaffold的
Kmer为35跑出来的效果更惨,203万的contig,近60万的scaffold。
我觉得问题可能不是这里了,可能是没有用到那个20k和3k的双端测序库,唉,其实我习惯了illumina的测序数据,不太喜欢这个454的
感觉组装好难呀,业余时间搞不定呀,希望有高手能一起交流,哈哈,我自己再慢慢来试试。